¡Bienvenidos a Alliance!
Una unidad para la ejecución y desarrollo de ensayos clínicos internacionales farmacéuticos y de dispositivos con más de 20 años de experiencia
Descubre nuestra historia
Sobre Nosotros
Generamos conocimiento científico desde hace más de 30 años. Con más de 250 estudios de investigación original y participación en 200 ensayos clínicos multinacionales de fases 2 y 3, colaboramos con prestigiosas compañías farmacéuticas y CRO’s para impulsar la innovación médica y garantizar resultados confiables.



Descubre Alliance Investigación
Misión
Ser el mejor sitio nacional de investigación e innovación de servicios y productos para la salud, conduciéndose con altos estándares en calidad, en valores y en principios; todos ellos bajo una conducta responsable en investigación. La integridad y el cuidado de los participantes de los proyectos serán nuestra prioridad. La apertura y la incorporación de los cambios tecnológicos y de la evolución de la investigación serán la base de nuestro desarrollo.
Visión
Ser en el 2028 el mejor centro de investigación e innovación farmacéutica y de dispositivos en el campo de la endocrinología, metabolismo y áreas afines. Liderando la investigación clínica en México; contribuyendo intensamente en la generación de alternativas para mejorar la salud; formando investigadores profesionales y contribuyendo con actividades que van mas allá de la conducción de ensayos clínicos.
Experiencia
La experiencia del fundador e investigador principal de este sitio de investigación (JGGG) es de mas de 25 años. Inició en el Servicio de Endocrinología del Hospital Universitario de la UANL en 1999. En el año 2004 inició la Subdirección de Investigación de la Facultad de Medicina de la UANL coordinando, junto con múltiples colaboradores en esta oficina, la investigación original y en vinculación con la industria que ocurría en esta institución, posición que dirigió hasta el año 2022. A lo largo de todo este tiempo fue investigador principal de más de 200 ensayos clínicos multinacionales hasta septiembre del 2025. Ha sido investigador principal en cerca de 200 estudios de investigación originales alcanzando mas de 8000 citaciones a sus estudios de investigación y alcanzando el nombramiento de Investigador Nacional nivel III emérito. Ha recibido múltiples reconocimientos a su carrera de investigador. Su equipo de colaboradores tiene también gran experiencia en investigación farmacéutica y original.
Nuestros Servicios
Ofrecemos servicios como

Ejecución de Ensayos Clínicos
Es la fase en la que se aplica el protocolo aprobado en participantes humanos. Incluye la administración del tratamiento, el seguimiento de los sujetos y la recolección sistemática de datos. Su objetivo es evaluar la seguridad y eficacia del producto en estudio.

Análisis de Tamaño de Muestra
Determina la cantidad adecuada de participantes necesarios en un estudio. Se basa en criterios estadísticos como el nivel de confianza, el poder del estudio y la variabilidad esperada. Su finalidad es asegurar resultados válidos y confiables sin usar más sujetos de los necesarios.

Estadística
Se recopila, analiza e interpreta los resultados, identifica patrones y comprueba la hipótesis de investigación. Es esencial para tomar decisiones basadas en evidencia científica.

Interpretación de Resultados
Analiza los datos para determinar si los objetivos del estudio se cumplieron y evaluar la validez de los hallazgos. Es clave para extraer conclusiones y apoyar la toma de decisiones.
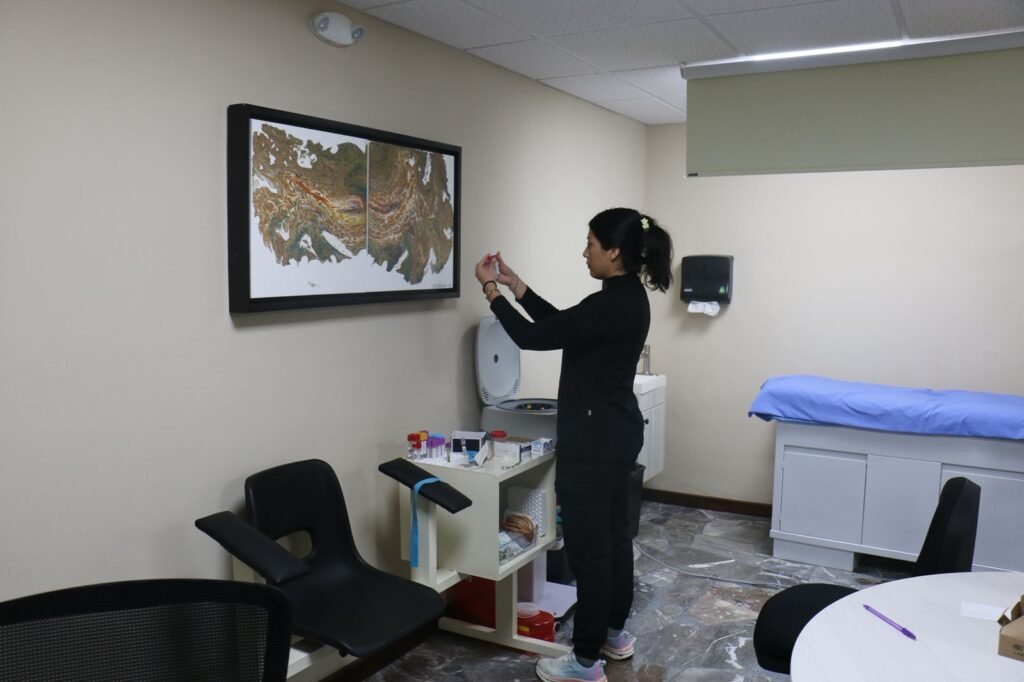
Determinación de Analitos y Hormonas
Implica la medición precisa de sustancias específicas en muestras biológicas. Se realiza mediante métodos de laboratorio validados para garantizar exactitud y confiabilidad. Es fundamental para el diagnóstico, seguimiento y evaluación clínica.

Edición y publicación de resultados en revistas internacionales con arbitraje
Se prepara y se somete, asegurando la calidad, validez y rigor metodológico del estudio, lo que permite la difusión del conocimiento científico a la comunidad internacional mediante la publicación de los resultados en revistas médicas internacionales con arbitraje.

Traducción de Ensayos Clínicos
Se adaptan documentos garantizando la correcta comprensión de protocolos, consentimientos y resultados. Es esencial para cumplir requisitos regulatorios y facilitar la colaboración internacional.

Cursos de buenas prácticas clínicas en investigación y formación de centros de excelencia
Capacitan al personal en normas éticas y científicas. Aseguran la correcta conducción de estudios clínicos y la protección de los participantes. Contribuyen al fortalecimiento institucional y a la calidad de la investigación.
Recursos Tecnológicos
Refrigeradores a 2 – 8 °C
Congelador a – 20 °C
Campana de flujo laminar
Cuarto a 20 °C permanente.
Acceso por reconocimiento facial.
Centrífugas
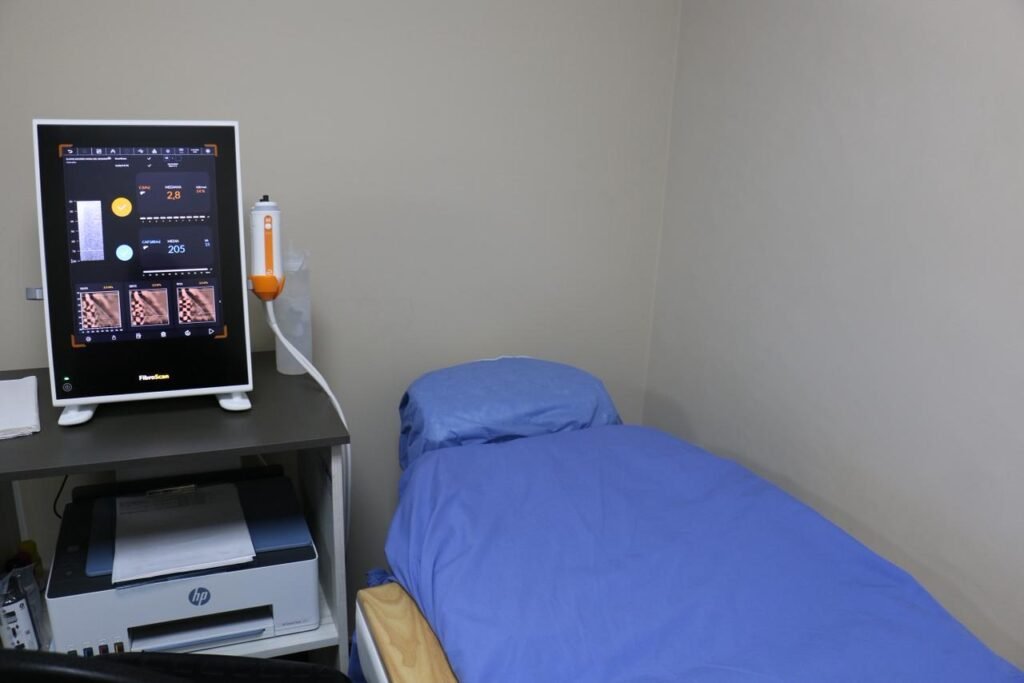
Fibroscan o elastograma hepático.
Electrocardiógrafo
Báscula a 250 kg.
Estadimetro a mm.
Batería de respaldo de 24 hrs.
Mesa de toma de muestras.
Carro rojo
Fotocopiadora, scan.
Internet de banda ancha.
Televisiones 75 in
Rayos inalámbricos.
Cámaras de seguridad.

Instalaciones Físicas
Recepción
Consultorios
Área de Criopreservación
Farmacia
Área de monitoreo
Gestión de muestras
Área de coordinadores
Sala de Juntas y de proyectos
Dirección
Cafetería
Almacenes
Estacionamiento



Recursos Humanos
4 Médicos investigadores
4 Coordinadores de estudio
1 Coordinadora de regulatorio
1 Enfermera en toma y manejo de muestras
1 Administradora
1 Contadora
1 Recepcionista
1 Auxiliar administrativo

1. ¿Qué es un estudio clínico de investigación?
Es una clase de estudio que se realiza principalmente con el propósito de determinar la eficacia, la seguridad y el metabolismo de medicamentos muy nuevos en seres humanos. Con estos estudios se obtiene la potencial autorización de un medicamento para tratar una enfermedad o prevenir sus complicaciones.
2. ¿Es muy seguro participar en uno de estos estudios?
Desde ya hace muchos años participar en un estudio de investigación es muy seguro. Los médicos responsables de estos estudios en todos los países tienen certificaciones y reconocimientos por Universidades y Sociedades médicas científicas y la experiencia para evaluar los riesgos de una persona que va a iniciarse en un estudio. Estos médicos muy reconocidos son seleccionados por la industria farmacéutica y son calificados y autorizados también por la COFEPRIS en el área de regulación sanitaria. La preparación académica y la experiencia de todos los que trabajan en un sitio de investigación son también evaluados y autorizados por cada uno de los miembros de los comités de ética y de investigación.
La persona que se decide en participar en un estudio de investigación deberá firmar la autorización para participar en un estudio (consentimiento informado) después de una explicación detallada de todas las características del estudio.
3. ¿Qué es lo que más protege a alguien que participa en un estudio?
La libertad plena de decidir participar y de retirarse de participar en el estudio en cualquier momento que lo deseara.
Sin embargo, los comités de ética y de investigación vigilan continuamente por el sano desempeño de los participantes del estudio y la protección de cualquier riesgo no calculado.
4. Consentimiento informado, ¿Qué es y para que sirve?
Nadie puede participar en un estudio de investigación si no firma su autorización para iniciar en un estudio.
Cualquier error en el llenado de este consentimiento es muy revisado y penalizado para el investigador y el sitio en que se realiza la investigación.
El consentimiento informado es un escrito que surgió hace muchas décadas precisamente para evitar cualquier tipo de abuso en una persona que participa en un estudio. Este documento es revisado muy minuciosamente por el comité de ética y por la COFEPRIS.
Es un documento de extensión variable, que detalla todas las características de un estudio, sus riesgos, la duración del estudio, su número de visitas, las responsabilidades que adquiere una persona en un estudio, los datos del investigador, y muchas cosas más. Debe ser firmado en cada hoja por el participante y por dos testigos imparciales al estudio.
5. ¿Quién puede participar en un estudio de investigación clínica?
Cualquier persona que desee participar en un estudio y que reúna las características indicadas por el investigador. A él o ella deberá de explicársele el consentimiento informado y de estar de acuerdo proceder a firmarlo.
6. ¿Quién patrocina los estudios clínicos?
Alguien debe pagar el costo de un ensayo clínico. Son estudios muy muy costosos porque habitualmente ocurren en muchos países, con muchas personas por participar, con muchos requisitos y con muchos exámenes de laboratorio y estudios de imagen.
Aunque habitualmente es una compañía farmacéutica nacional o internacional, en algunos países es patrocinado por Universidades, sociedades sin beneficio económico y autoridades sanitarias.
7. ¿Qué es un placebo?
El placebo es una sustancia innerte o inactiva con las mismas características de presentación y vía de administración que la medicina en estudio. Se utiliza en investigación para comparar los resultados con un medicamento activo en investigación.
El placebo da validez a los resultados de un medicamento en estudio.
8. ¿Qué es un estudio ciego?
El ciego es un elemento que en investigación le da validez o veracidad a los resultados de un estudio. Evita que el paciente, el investigador o la compañía dueña de la medicina sesguen la apreciación del efecto del medicamento en estudio. En los estudios de investigación lo mas habitual es que la persona que participa, el investigador y la compañía ignoren si el participante está recibiendo el medicamento en estudio o placebo. Como mecanismo de seguridad del participante, con debida autorización se puede “romper el ciego” o sea, determinar si el participante está tomando placebo o medicamento activo.
9. ¿Qué tengo que hacer si quiero abandonar un estudio clínico?
El retirar la participación de una persona es algo que puede llegar a afectar muy seriamente a un estudio. Si el motivo es algo que se puede corregir será muy valioso resolverlo. Por ejemplo, falta de comunicación con el investigador, tardanza en atenderlo, etc. Si no es posible resolver la dificultad, una alternativa es dejar de tomar el medicamento en estudio, pero mantener comunicación con el investigador hasta el final del estudio. Si no desea continuar de ninguna forma, el participante puede hacerlo en cualquier momento, incluso sin dar una explicación del por qué.
10. ¿Que significa aleatorización?
Aleatorio significa al azar. La aleatorización se utiliza en investigación para asignar la participación de alguien a medicamento activo o a placebo. Hay muchas formas de aleatorizar a una persona. Lo mejor es usar la tabla de números aleatorios. El principal atributo de esto es balancear todas las características de los participantes a que sean iguales o no diferentes en sus características; que sean comparables a la hora de analizarlos.
11. ¿Qué es un evento adverso?
Es cualquier reacción que ocurre en el participante después de haber firmado su consentimiento informado de participación voluntaria, aun y cuando todavía no reciba ningún medicamento en experimentación.
Los eventos adversos serios requieren especial atención por los comités de ética y por el patrocinador. Estos incluyen: pone en riesgo la vida del paciente, que obliga a que el participante sea internado en hospital, que genere alguna discapacidad o en caso de tomarlo durante un embarazo lleve a una anomalía congénita.
12. ¿Es necesario realizar investigación?
La medicina no hubiera avanzado si no fuera por que se realiza investigación. Si no hubiera investigación todavía estuviéramos utilizando remedios que no han probado ser eficaces. Gracias a la investigación existen antibióticos, medicamentos para la diabetes, para la elevación del colesterol, para la osteoporosis, etc.
13. En un estudio de investigación los participantes son “conejillos de Indias”
Este es un viejo tabú que ha impedido en mayor o menor grado la participación de personas en estudios de investigación. Es algo muy negativo. Es una forma no informada de descalificar a la investigación médica de fármacos. Nadie en estudios de investigación autorizada está siendo un conejillo de indias. Todos los participantes están muy vigilados y protegidos por los investigadores, los comités de ética e investigación y por las autoridades sanitarias.
Nuestro Personal

Dr. Med José Gerardo González
Investigador Prinicipal

Dr. PhD René Rodríguez Gutiérrez
Investigador Prinicipal

Dra. Sandra Garza Félix
Investigadora

Dra. Alicia Carolina Dávila Batista
Investigadora

Dr. Andrés Ledesma Caballero
Investigador

QCB Rocío Karina Vidales Sifuentes
Coordinadora

Lic. Enf. Natalia G. Rivera Almaguer
Coordinadora

Lic. Enf. Claudia Y. Morales Hernández
Coordinadora

Lic. Enf. Alicia Cepeda Hernández
Coordinadora

Lic. Enf. José Ernesto Sánchez Cordero
Coordinador

Olivia Alfaro Romero
Administración

Ana Laura Galván Garza
Recepción

Miguel A. Hernández López
Auxiliar Administrativo
Contacto
A continuación, le indicamos cómo ponerse en contacto con nosotros para resolver cualquier duda o consulta.
Zapotlán 126, Mitras Sur, 64020 Monterrey, N.L.
81-2633-5201
allianceinvestigacion@gmail.com
Escríbenos
Envíanos un mensaje para resolver todas tus dudas.
